解决方案
Solution Center
联系我们
Contact Us
 山东科派环保设备有限公司
山东科派环保设备有限公司地址:山东潍坊安丘经济开发区
销售热线:13563633138
18866361777
电话:0536-2255318
传真:0536-2255519
网址:http://www.sdfdhj.com
邮�䣺sdkepai@163.com
 您现在的位置:首页->脱硫脱硝除尘解决方案
您现在的位置:首页->脱硫脱硝除尘解决方案脱硫脱硝除尘解决方案
一、提出背景
随着世界各国工业化进程的不断加深,SO2、NOX污染已超过烟尘污染成为大气环境的第一大污染物。烟气脱硫(FGD)有别于其他脱硫方式是世界上唯一大规模商业化应用的脱硫方法,是控制酸雨和SO2污染的最为有效的和主要的技术手段。
目前,世界各国对烟气脱硫都非常重视,已开发了数十种行之有效的脱硫技术,其中广泛采用的烟气脱硫技术有:
(1)石灰/石灰石—湿法。
(2)旋转喷雾半干法(LSD)。
(3)炉内喷钙增湿活化法(LIFAC)。
(4)海水烟气脱硫法。
(5)氨法烟气脱硫。
(6)简易湿式脱硫除尘一体化技术。
石灰/石灰石—石膏湿法,具有适用煤种宽、原料廉价易得、脱硫率高(可达90%以上)等诸多优点,占据最大的市场份额,但投资和运行费用大,运行维护量大。
旋转喷雾法脱硫率较湿法低(能达到80%—85%),投资和运行费用也略低于湿法。产物为亚硫酸钙(CaSO3)。
炉内喷钙尾部增湿法,脱硫率可达70%—80%,工程造价较低。产物为亚硫酸钙(CaSO3),易造成炉内结渣。
海水烟气脱硫技术,工艺简单,系统运行可靠,脱硫率高(可达90%以上)运行费用低。脱硫系统需要设置在海边且海水温度较低,溶解氧(OC)较高。
氨法除硫通常以合成氨为原料,产物为硫氨等。需要邻近合成氨工厂及化肥厂。
简易湿式脱硫除尘一体化技术,脱硫率低(60%左右),造价较低原料为工业废碱及烧碱,需要临近有废碱液排放的工厂,中和后,废水需排入污水厂进行处理。
烟气脱硫的技术及装置虽然日臻完善,但在大多数国家,尤其是在能源结构中煤炭占较大比例的国家中,其推广和普及却举步唯艰,拿我国来说,近20年来花巨资引进的技术和装置难以推广,巨额的投资和高昂的运行费用使企业背上了沉重的负担,难以承受。所以说具有真正推广普及意义的技术和装置还有待于继续研究和开发。
在现在国际国内市场竞争异常激烈的条件下,要研究开发一种新的技术和设备装置,使其能大规模普及应用,应具备以下几个特征:
(1)原料(中和剂)廉价易得,脱硫率高。
(2)工程投资和运行费用要低到应用企业能承担得了。
(3)工艺流程简单,运行可靠,易于调控且对锅炉正常运行无不良影响。
(4)对各种含硫煤(油)具有较好的适应性。
(5)不造成二次污染,诸如水污染、粉尘、噪声等。
二、推理分析
(1)原料(中和剂)
随着市场经济的发展和社会的进步,原来意义上的百年老店越来越少,每年都有大量的新兴产业掘起,每年都有大量的老产业退出市场。
烟气脱硫项目一般都需要投入大量资金,如果原料和工艺依赖于临近的工厂(如合成氨、化肥、废碱排放等),那么这个项目很可能由于这些工厂的关停并转而中途停止运转,使该项目投资得不到应有的经济和社会效益。所以以石灰石、石灰为中和剂的烟气脱硫技术为大多数业内专家所认同。以石灰为中和剂成本高于石灰石,且需要设备、构筑物及监测设备较多;使用石灰石成本低且反应易于控制,是最具实用性的中和剂。
传统的“石灰石—石膏法烟气脱硫”需要将石灰石粉磨至200—300目,这样就需要建一座粉磨站,既增加投资,又造成了一定程度的“噪声”和“粉尘”污染,且其产物与反应物混合在一起,造成钙硫比的提高,增加了运行费用。如果采用脱硫脱硝除尘一体化技术,即可实现脱硫脱硝除尘同时在一个装置内完成,具有设备简单、投资小、运行费用低,大幅度提高经济效益。
(2)产物
湿法脱硫,脱硫率最高(可达90%以上),中和产物有两种,硫酸钙CaSO4和亚硫酸钙CaSO3,通常是两种物质的混和物,中和产物被完全再利用的可能性不大,如果亚硫酸钙(CaSO3)一但进入水体,由于它具有很强的还原性,会迅速耗尽水中的溶解氧,使水中鱼类大量死亡,甚至灭绝,因为它溶解速度很慢,其污染物会在很长时间内存在,严重破坏水体生态环境,所以中和产物中不含亚硫酸钙(CaSO3)最为安全,既可再利用创造价值也可安全排放。
(3)钙硫比
钙硫比(Ca/S)是决定运行费用的重要因素,Ca/S=1是经济运行的极限状态,也就是说哪种脱硫工艺Ca/S实现或接近1,那么它就可能实现真正意义的经济运行。目前的湿法脱硫,剩余反应物与脱硫产物混合在一起被排除掉无法分离,所以很难实现理想的Ca/S, 如果反应物以颗粒状态存在,解决这个问题,实现理想的Ca/S较为容易,而且设备和资金投入也随之减少,有利于实现真正意义的经济运行。
三、理想模型
综上所述,最理想的烟气脱硫工艺应该是:
(1)湿法脱硫(脱硫率可达90%以上)。
(2)中和剂为石灰石。
(3)钙硫比(Ca/S)为1。
(4)产物为硫酸钙且不含亚硫酸钙杂质。
(5)投资少,工艺简单,运行费用低廉,无二次污染。
(6)控制参数少,测控设备成熟,可实现全线自动控制。
(7)运行中的中间循环物质由锅炉及电厂废液补充,对周边企业无依赖性。
(8)充分吸收与利用烟气余热。
这个理想的模型如果能够实现,很可能成为烟气脱硫技术中最为理想的运行模式,它的推广和应用可以创造巨大的市场机会和社会价值,但要真正实现这种理想模式却很难,主要原因是:
(1)石灰石颗粒要迅速溶解,PH值必须小于4,但PH值小于4时CaCO3的溶解物对SO2几乎不吸收。
(2)SO2溶于水生成的H2SO3及被氧化生成的H2SO4,与石灰石颗粒反应后生成的CaSO3和CaSO4会附着在石灰石颗粒的表面,而且越反应堆积越多,使反应很难继续进行下去。
(3)CaSO4与CaSO3同为吸收产物,使CaSO4析出且不产生CaSO3是比较困难的。
可以说这3个问题是“石灰石法”脱硫的真正的难以愈越的天险,能否解决这3个问题是这个工艺能否达到预定目标及其装置能否稳定运行的关键。
四、循环架桥理论
既然是天险就应该架起一座桥梁把它愈越过去,经研究发现脱硫脱硝除尘一体化技术具有架桥作用。脱硫脱硝除尘一体化技术,系环保技术领域烟气净化技术。它是通过烟水混合器利用二次喷射原理把烟吸入水中,在均匀溶解器中将烟气和水进行充分地均匀地混合和溶解,从而使烟气中的飞灰和颗粒被水吸湿而沉淀,有害气体溶于水中,利用化学方法清除烟气中的SO2、NOX和粉尘。这种方法是通过附图所示的工作原理图来实现的。它的除尘效率100%;脱硫效率>98%;脱销效率>90%以上。它的烟气混合器同时又是一台引风机。它适用于燃煤(汽、油)锅炉及各种工业窑炉等的烟气净化技术工程。系统结构简单,成本低,性能价格比高,节能,耐高温,寿命长。
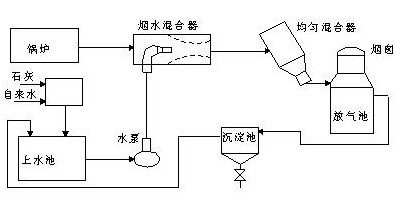
系统的技术特征简介
1)结构简单设备少(如图1)
烟水混合器:由水喷管和拉法尔喷管组成,构成二级喷射机构。用于把烟气吸入水中。
均匀溶解器:是一种洗烟设备,用于把烟全部溶于弱碱水中,灰尘被水弄湿而变重,有害气体和碱起化学反应生成盐。
水泵:动力设备。
水池:上水池,沉淀池和下水放气池。
2)适合于多种工艺流程(详细见附件)
废物丢弃法:适用于各种规格的燃煤(油、气)锅炉;燃煤中含硫量小;采用脱硫脱硝除尘一体化工艺流程。石灰、石灰石作脱硫剂。
回收石膏法:适用于各种规格的燃煤(油、气)锅炉,燃煤中含硫量大;采用脱硫脱硝除尘一体化工艺流程。石灰作脱硫剂。
回收化肥法:适用于各种规格的燃煤(油、气)锅炉,燃煤中含硫量大;采用脱硫脱硝除尘一体化工艺流程。气氨、氨水或固体碳酸氢铵作吸收剂。
除尘效率100%;脱硫效率>97%;脱硝效率>90%以上。适用于炼钢厂、水泥厂等工业窑炉。耐高温寿命长。
3)防腐措施
溶液配置:溶液配置成呈碱性,避免酸存在于溶液中。如图1所示,稀碱溶液连续均匀地加入到上水池循环液中,使其PH值保持在8-9之间,在均匀溶解器中碱溶液中的碱和烟气中的SO2等酸性氧化物反应生成盐。在沉淀池中溶液的PH值保持在7-8之间。溶液保持弱碱性,腐蚀性最小。
选择耐酸耐碱材料:不锈钢、陶瓷、耐火材料等耐磨耐酸碱材料。
对溶液的PH值自动进行监控监测。
4)废物排除系统
沉淀池设计成圆形,底部成漏斗形,安装沉淀物收集器使浓度大的浆液集中在漏斗中,用泥浆泵抽出。泥浆中的废水澄清后循环使用。
丢弃物用于建筑材料,石膏用于工业,肥料用于农业。
五、石膏法工作原理图
前级用于干法除尘器(如电除尘器等)除去>90%的粉尘,便于回收再用,后级采用脱硫脱硝除尘一体化技术(本方案),除尘效率100%;脱硫效率>97%,脱硝效率>90%以上,并将SO2转化为石膏。
1、石膏法的工艺流程图

2、化学反应方程式如下
Ca(OH)2+SO2=CaSO3+H2O
2CaSO3+O2=2CaSO4
CaSO3+1/2H2O=CaSO3•1/2H20
CaSO4+2H2O=CaSO4•2H2O
CaSO3•1/2H20+O2+2H2O=2CaSO4•2H2O
NO+NO2+H2O+O2=2HNO3
Ca(OH)2+2HNO3=Ca(NO3)2+H2O
六、回收化肥法(氨-亚硫酸铵法)适用范围
适用于各种规格的燃煤(油、气)锅炉;燃煤中含硫量大;采用脱硫脱硝除尘一体化,除尘器效率100%;脱硫效率>98%;脱销效率90%工艺流程。气氨、氨水或固体碳酸氢铵作吸收剂。
工艺流程图
1、固体碳酸氢铵作为氨源的工艺流程图如下:
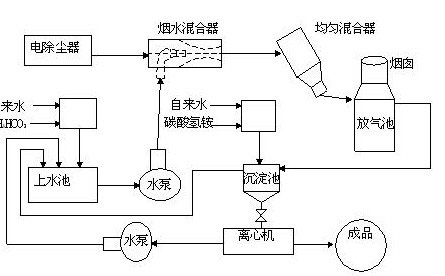
2、氨水作为氨源的工艺流程图如下:
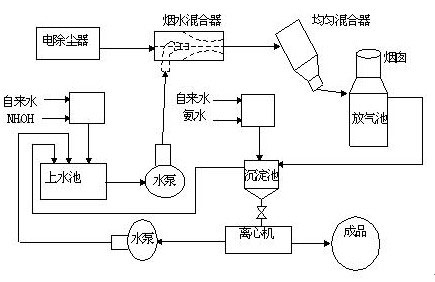
3、脱硫工艺流程说明
化学反应方程式如下:
2NH4HCO3+SO2=(NH4)2SO3+H2O+2CO2 (A)
(NH4)2SO3+SO2+H2O=2NH4HSO3 (B)
吸收过程以(B)式为主,而2NH4HSO3在产生过程中只是补入吸收系统使部分2NH4HSO3再生为(NH4)2SO3,以保持循环吸收液碱度(SO2/NH3)基本不变。
若烟气中有氧,则(NH4)2SO3+O2/2=(NH4)2SO4。通常烟气中含有少量SO3,则有:
NH4HCO3+SO2+H2O=(NH4)2SO4+ NH4HSO3。NH4HSO3呈酸性。需加固体碳酸氢铵中和后,使NH4HSO3转变为(NH4)2SO4;
NH4HSO3+ NH4HCO3= NH4HSO3•H2O+CO2 (C)
(C)式为吸热反应,溶液不经冷却即可降到0℃左右。由于(NH4)2SO3比NH4HSO3在水中的溶解度大,则溶液中NH4HSO3•H2O过饱和结晶析出,将此溶液经离心分离可制得固体亚铁。
七、脱销工艺流程说明
1、何为脱硝?所谓脱硝,指的是除去烟气中的NOX,NOX主要是NO和NO2组成,而NO含量占90%以上。要除去烟气中的NO和NO2,就必须研究NO和NO2的性质。
NO是一种惰性氧化物,它虽然溶于水,但不能生成氮的含氧酸。在0℃时,一体积水可溶解0.07体积的NO。NO最特殊的化学性质是加合作用,在常温下能与空气中的氧化合,生成红棕色的NO2。NO是不稳定的,和O2相遇,能使O2分裂成氧原子,并和其中的一个氧原子结合成NO2。
NO2是红棕色有特殊臭味的气体,在-10℃左右聚合成N2O4,在120℃时N2O4全部分解成NO2,温度再高NO2开始分解成NO和O2。NO2是一种强氧化剂,它能把SO2氧化成SO3。NO2溶于水生成硝酸和亚硝酸。NO2的毒性是NO的5倍。
NO和NO2是怎样产生的呢?一般情况下N2和O2不发生化合反应。氮氧化合物是在空气中放电时或在高温燃烧过程中产生的,首先生成NO,然后由NO氧化成NO2。在高温燃烧过程中空气中的氮和燃料中的氮化物等不可能燃烧的物质与氧起化学反应,首先形成NO,随后它的一部分在烟道内与氧化合形成NO2,大部分的NO从烟囱中排入大气,并与大气中的氧结合成NO2。而未被氧化成NO2的NO就在大气中与NO2共存下来。
在燃烧过程中燃烧气体温度越高,过剩空气越多,形成NO量就越多。即在燃烧效率越高的情况下,NO越容易生成。这种燃烧方式生成的NOX中NO占90%以上,NO2较少。
按照常用的燃烧方式。煤的燃烧物中NOX的含量为500-1500ppm。
2、湿法脱硝
脱硝方法分为干法和湿法两种。干法脱硝效率在80%左右,且成本较高。这里采用湿法脱硝。
NO2溶于水生成硝酸和NO:
3NO2+H2O=2HNO3+NO
当氧气足够时:
4NO2+O2+2H2O=4HNO3
NO虽然溶于水,但不能生成氮的含氧酸。在0℃时,一体积水可溶解0.07体积的NO。NO难溶于水成为脱硝的难点。但在“脱硫脱硝除尘一体化技术”中有足够的水使NO溶于水中,有关研究表明当水溶液中硝酸含量>12%时,NO的溶解度比在纯水中大100倍,即一体积水能溶解7体积的NO。设烟气开始溶于水中时水是纯净,首先是NO2溶于水中生成HNO3,如果NO2在水中不被还原,按照“脱硫脱硝除尘一体化技术”中烟水的比例计算,2小时44分钟后,水溶液中硝酸的含量将为12%左右。因此可以说NO溶于水中是不成问题的。
NO和NO2既然都已溶于水中。采用还原法将它们还原成N2气。还原法使用的还原剂为(NH4)2SO3和NH4HSO3,它们正是氨法脱硫工艺中的产物。还原剂就已在溶液中,脱硝就已经在均匀溶解器中悄悄地进行着。因为NOX在烟气中的数量都很小,还原剂(NH4)2SO3和NH4HSO3的数量是足够的。如果NOX的数量不能全部被还原,剩余的部分将变成NH4NO3被留在溶液中和(NH4)2SO4一起被从溶液中分离出来做为化肥。它们化学反应方程式为:
2NO+O2=2NO2+27千卡
NO+NO2+H2O=4HNO2
NO2+2H2O=HNO2+HNO3
4NO2+O2+2H2O=4HNO3
NH3+HNO3=NH4NO3
NH3+HNO2=N2+2H2O
NH4OH+HNO3=NH4NO3+H2O
NH4OH+HNO2=N2+3H2O
NH4OH+NH4HSO4=(NH4)2SO4•H2O
3、脱硫脱硝除尘效果
1)脱硫率:98%
2)脱硝率:90%
3)除尘效率:100%
八、技术工艺特点
(1)造价和运行费用极低,运行管理工作量极少。
(2)工艺简单,可实现全程自动化控制。
(3)测控参数少(PH值、温度、液位),测控技术成熟。
(4)各流程均有成熟技术可借鉴。
(5)适合各种规模的电站及工业锅炉。
(6)对各种含硫煤(油)具有较好的适应性。
(7)对燃烧装置无不良影响,生产工艺、原料来源及产物应用对周边企业无依赖性。
(8)有利于烟气余热的吸收和利用。
(9)不造成(水体、噪声、粉尘等)二次污染。
(10)脱硫脱硝除尘在同一个装置内完成。一次性投资,脱硫率98%,脱硝率90%以上,除尘率100%,均可进行达标排放。
(11)运行费用低。比传统脱硫方法降低运行费用50%-80%左右。
九、烟气脱硫降低费用
目前的烟气脱硫技术存在最大的问题是技术复杂,造价高,运行费用大。一台300MW(30万千瓦)发电机组烟气脱硫,一般采用比较成熟的石灰石--石膏湿法烟气脱硫,脱硫效率95%左右,每年减少二氧化硫排放量约1万吨,每脱除1万吨二氧化硫的能力建设投资约1~1.5亿元,电厂烟气脱硫设施的运行耗电量较大,一年的脱硫剂、用电和人工等运行费在1600万元左右,摊到每度电的脱硫费用约0.03元,而上网电价的脱硫补贴只有0.015元。现时几十吨的锅炉多数用双碱法,近年烧碱(用作烟气脱硫剂)的销售价成倍提高,脱硫运行费用随之大幅度升高。在煤价升幅50%多和竞价上网的双重压力下,加上脱硫补贴缺口大,高成本的脱硫设施能否坚持正常运行面临严峻的考验。
我国脱硫产业常常面临脱硫运行成本高,国家补贴的脱硫电价,无法使脱硫装置保本运行,采用本技术后,能使目前脱硫系统因运行成本高而停用的SO2净化设备进行运转,真正实现脱硝运行费用“零”投资,无成本,大幅度降低运行费用,大量节约水资源,节约电厂传统脱硫技术因磨损大、结垢严重、系统复杂、配套设备多、维护工作量大,和脱硫系统因(石灰乳法)脱硫堵塞、结垢、腐蚀、磨损、运行费用高、耗电量大给厂内造成的巨大损失,真正实现节能减排,提高效益,可取消浆液循环泵,取消氧化风机,取消制浆系统,取消石灰石球磨机等,大大节约系统的用电量,本脱硫方法与传统的(石灰乳)脱硫方法相比,脱硫效率98%以上,脱硝效率90%以上,可降低运行费用50%-80%,是脱硫领域的一次创新和一项重大突破,在国内外尚属首创。无论对低硫煤、中硫煤、高硫煤,均能达到与传统(石灰乳)法脱硫相当的效果,实现脱硫系统运行费用零投资,无成本脱硫,脱硫塔排出的吸收液,重复利用,循环脱硫,即节约了大量的水资源,又减少了脱硫系统设备系统管道的堵塞和结垢,省去了传统湿法脱硫工艺中庞大的制浆系统,省去了废液和废水处理设备,整套系统大为简化,设备投资大为降低。
十、烟气脱硫技术对比
与传统的石灰乳脱硫方法脱硫相比,即解决了用水量大,浪费水资源,系统容易结垢、堵塞等问题,又可解决脱去烟气中SO2的问题,一举两得,脱硫效率97%以上,脱硝效率90%以上,除尘率100%,不需大的投资建设脱硝设备,无成本,大幅度降低运行费用,提高经济效益,真正实现节能减排,循环经济,变废为宝,实现国家可持续发展。
十一、社会经济意义
湿法脱硫技术是最具商业优势的脱硫技术,“脱硫脱硝除尘一体化技术”使(湿法)烟气脱硫设备及装置的小型化、普及化成为可能,使治理SO2污染在一些经济条件较差的国家和地区的普及应用成为可能。它的经济、高效、节能、环保、集控的特点和优点有利于为众多企业所接受,为经济的可持续发展和环境科技的进步做出应有的贡献。
随着世界各国工业化进程的不断加深,SO2、NOX污染已超过烟尘污染成为大气环境的第一大污染物。烟气脱硫(FGD)有别于其他脱硫方式是世界上唯一大规模商业化应用的脱硫方法,是控制酸雨和SO2污染的最为有效的和主要的技术手段。
目前,世界各国对烟气脱硫都非常重视,已开发了数十种行之有效的脱硫技术,其中广泛采用的烟气脱硫技术有:
(1)石灰/石灰石—湿法。
(2)旋转喷雾半干法(LSD)。
(3)炉内喷钙增湿活化法(LIFAC)。
(4)海水烟气脱硫法。
(5)氨法烟气脱硫。
(6)简易湿式脱硫除尘一体化技术。
石灰/石灰石—石膏湿法,具有适用煤种宽、原料廉价易得、脱硫率高(可达90%以上)等诸多优点,占据最大的市场份额,但投资和运行费用大,运行维护量大。
旋转喷雾法脱硫率较湿法低(能达到80%—85%),投资和运行费用也略低于湿法。产物为亚硫酸钙(CaSO3)。
炉内喷钙尾部增湿法,脱硫率可达70%—80%,工程造价较低。产物为亚硫酸钙(CaSO3),易造成炉内结渣。
海水烟气脱硫技术,工艺简单,系统运行可靠,脱硫率高(可达90%以上)运行费用低。脱硫系统需要设置在海边且海水温度较低,溶解氧(OC)较高。
氨法除硫通常以合成氨为原料,产物为硫氨等。需要邻近合成氨工厂及化肥厂。
简易湿式脱硫除尘一体化技术,脱硫率低(60%左右),造价较低原料为工业废碱及烧碱,需要临近有废碱液排放的工厂,中和后,废水需排入污水厂进行处理。
烟气脱硫的技术及装置虽然日臻完善,但在大多数国家,尤其是在能源结构中煤炭占较大比例的国家中,其推广和普及却举步唯艰,拿我国来说,近20年来花巨资引进的技术和装置难以推广,巨额的投资和高昂的运行费用使企业背上了沉重的负担,难以承受。所以说具有真正推广普及意义的技术和装置还有待于继续研究和开发。
在现在国际国内市场竞争异常激烈的条件下,要研究开发一种新的技术和设备装置,使其能大规模普及应用,应具备以下几个特征:
(1)原料(中和剂)廉价易得,脱硫率高。
(2)工程投资和运行费用要低到应用企业能承担得了。
(3)工艺流程简单,运行可靠,易于调控且对锅炉正常运行无不良影响。
(4)对各种含硫煤(油)具有较好的适应性。
(5)不造成二次污染,诸如水污染、粉尘、噪声等。
二、推理分析
(1)原料(中和剂)
随着市场经济的发展和社会的进步,原来意义上的百年老店越来越少,每年都有大量的新兴产业掘起,每年都有大量的老产业退出市场。
烟气脱硫项目一般都需要投入大量资金,如果原料和工艺依赖于临近的工厂(如合成氨、化肥、废碱排放等),那么这个项目很可能由于这些工厂的关停并转而中途停止运转,使该项目投资得不到应有的经济和社会效益。所以以石灰石、石灰为中和剂的烟气脱硫技术为大多数业内专家所认同。以石灰为中和剂成本高于石灰石,且需要设备、构筑物及监测设备较多;使用石灰石成本低且反应易于控制,是最具实用性的中和剂。
传统的“石灰石—石膏法烟气脱硫”需要将石灰石粉磨至200—300目,这样就需要建一座粉磨站,既增加投资,又造成了一定程度的“噪声”和“粉尘”污染,且其产物与反应物混合在一起,造成钙硫比的提高,增加了运行费用。如果采用脱硫脱硝除尘一体化技术,即可实现脱硫脱硝除尘同时在一个装置内完成,具有设备简单、投资小、运行费用低,大幅度提高经济效益。
(2)产物
湿法脱硫,脱硫率最高(可达90%以上),中和产物有两种,硫酸钙CaSO4和亚硫酸钙CaSO3,通常是两种物质的混和物,中和产物被完全再利用的可能性不大,如果亚硫酸钙(CaSO3)一但进入水体,由于它具有很强的还原性,会迅速耗尽水中的溶解氧,使水中鱼类大量死亡,甚至灭绝,因为它溶解速度很慢,其污染物会在很长时间内存在,严重破坏水体生态环境,所以中和产物中不含亚硫酸钙(CaSO3)最为安全,既可再利用创造价值也可安全排放。
(3)钙硫比
钙硫比(Ca/S)是决定运行费用的重要因素,Ca/S=1是经济运行的极限状态,也就是说哪种脱硫工艺Ca/S实现或接近1,那么它就可能实现真正意义的经济运行。目前的湿法脱硫,剩余反应物与脱硫产物混合在一起被排除掉无法分离,所以很难实现理想的Ca/S, 如果反应物以颗粒状态存在,解决这个问题,实现理想的Ca/S较为容易,而且设备和资金投入也随之减少,有利于实现真正意义的经济运行。
三、理想模型
综上所述,最理想的烟气脱硫工艺应该是:
(1)湿法脱硫(脱硫率可达90%以上)。
(2)中和剂为石灰石。
(3)钙硫比(Ca/S)为1。
(4)产物为硫酸钙且不含亚硫酸钙杂质。
(5)投资少,工艺简单,运行费用低廉,无二次污染。
(6)控制参数少,测控设备成熟,可实现全线自动控制。
(7)运行中的中间循环物质由锅炉及电厂废液补充,对周边企业无依赖性。
(8)充分吸收与利用烟气余热。
这个理想的模型如果能够实现,很可能成为烟气脱硫技术中最为理想的运行模式,它的推广和应用可以创造巨大的市场机会和社会价值,但要真正实现这种理想模式却很难,主要原因是:
(1)石灰石颗粒要迅速溶解,PH值必须小于4,但PH值小于4时CaCO3的溶解物对SO2几乎不吸收。
(2)SO2溶于水生成的H2SO3及被氧化生成的H2SO4,与石灰石颗粒反应后生成的CaSO3和CaSO4会附着在石灰石颗粒的表面,而且越反应堆积越多,使反应很难继续进行下去。
(3)CaSO4与CaSO3同为吸收产物,使CaSO4析出且不产生CaSO3是比较困难的。
可以说这3个问题是“石灰石法”脱硫的真正的难以愈越的天险,能否解决这3个问题是这个工艺能否达到预定目标及其装置能否稳定运行的关键。
四、循环架桥理论
既然是天险就应该架起一座桥梁把它愈越过去,经研究发现脱硫脱硝除尘一体化技术具有架桥作用。脱硫脱硝除尘一体化技术,系环保技术领域烟气净化技术。它是通过烟水混合器利用二次喷射原理把烟吸入水中,在均匀溶解器中将烟气和水进行充分地均匀地混合和溶解,从而使烟气中的飞灰和颗粒被水吸湿而沉淀,有害气体溶于水中,利用化学方法清除烟气中的SO2、NOX和粉尘。这种方法是通过附图所示的工作原理图来实现的。它的除尘效率100%;脱硫效率>98%;脱销效率>90%以上。它的烟气混合器同时又是一台引风机。它适用于燃煤(汽、油)锅炉及各种工业窑炉等的烟气净化技术工程。系统结构简单,成本低,性能价格比高,节能,耐高温,寿命长。

系统的技术特征简介
1)结构简单设备少(如图1)
烟水混合器:由水喷管和拉法尔喷管组成,构成二级喷射机构。用于把烟气吸入水中。
均匀溶解器:是一种洗烟设备,用于把烟全部溶于弱碱水中,灰尘被水弄湿而变重,有害气体和碱起化学反应生成盐。
水泵:动力设备。
水池:上水池,沉淀池和下水放气池。
2)适合于多种工艺流程(详细见附件)
废物丢弃法:适用于各种规格的燃煤(油、气)锅炉;燃煤中含硫量小;采用脱硫脱硝除尘一体化工艺流程。石灰、石灰石作脱硫剂。
回收石膏法:适用于各种规格的燃煤(油、气)锅炉,燃煤中含硫量大;采用脱硫脱硝除尘一体化工艺流程。石灰作脱硫剂。
回收化肥法:适用于各种规格的燃煤(油、气)锅炉,燃煤中含硫量大;采用脱硫脱硝除尘一体化工艺流程。气氨、氨水或固体碳酸氢铵作吸收剂。
除尘效率100%;脱硫效率>97%;脱硝效率>90%以上。适用于炼钢厂、水泥厂等工业窑炉。耐高温寿命长。
3)防腐措施
溶液配置:溶液配置成呈碱性,避免酸存在于溶液中。如图1所示,稀碱溶液连续均匀地加入到上水池循环液中,使其PH值保持在8-9之间,在均匀溶解器中碱溶液中的碱和烟气中的SO2等酸性氧化物反应生成盐。在沉淀池中溶液的PH值保持在7-8之间。溶液保持弱碱性,腐蚀性最小。
选择耐酸耐碱材料:不锈钢、陶瓷、耐火材料等耐磨耐酸碱材料。
对溶液的PH值自动进行监控监测。
4)废物排除系统
沉淀池设计成圆形,底部成漏斗形,安装沉淀物收集器使浓度大的浆液集中在漏斗中,用泥浆泵抽出。泥浆中的废水澄清后循环使用。
丢弃物用于建筑材料,石膏用于工业,肥料用于农业。
五、石膏法工作原理图
前级用于干法除尘器(如电除尘器等)除去>90%的粉尘,便于回收再用,后级采用脱硫脱硝除尘一体化技术(本方案),除尘效率100%;脱硫效率>97%,脱硝效率>90%以上,并将SO2转化为石膏。
1、石膏法的工艺流程图

2、化学反应方程式如下
Ca(OH)2+SO2=CaSO3+H2O
2CaSO3+O2=2CaSO4
CaSO3+1/2H2O=CaSO3•1/2H20
CaSO4+2H2O=CaSO4•2H2O
CaSO3•1/2H20+O2+2H2O=2CaSO4•2H2O
NO+NO2+H2O+O2=2HNO3
Ca(OH)2+2HNO3=Ca(NO3)2+H2O
六、回收化肥法(氨-亚硫酸铵法)适用范围
适用于各种规格的燃煤(油、气)锅炉;燃煤中含硫量大;采用脱硫脱硝除尘一体化,除尘器效率100%;脱硫效率>98%;脱销效率90%工艺流程。气氨、氨水或固体碳酸氢铵作吸收剂。
工艺流程图
1、固体碳酸氢铵作为氨源的工艺流程图如下:

2、氨水作为氨源的工艺流程图如下:

3、脱硫工艺流程说明
化学反应方程式如下:
2NH4HCO3+SO2=(NH4)2SO3+H2O+2CO2 (A)
(NH4)2SO3+SO2+H2O=2NH4HSO3 (B)
吸收过程以(B)式为主,而2NH4HSO3在产生过程中只是补入吸收系统使部分2NH4HSO3再生为(NH4)2SO3,以保持循环吸收液碱度(SO2/NH3)基本不变。
若烟气中有氧,则(NH4)2SO3+O2/2=(NH4)2SO4。通常烟气中含有少量SO3,则有:
NH4HCO3+SO2+H2O=(NH4)2SO4+ NH4HSO3。NH4HSO3呈酸性。需加固体碳酸氢铵中和后,使NH4HSO3转变为(NH4)2SO4;
NH4HSO3+ NH4HCO3= NH4HSO3•H2O+CO2 (C)
(C)式为吸热反应,溶液不经冷却即可降到0℃左右。由于(NH4)2SO3比NH4HSO3在水中的溶解度大,则溶液中NH4HSO3•H2O过饱和结晶析出,将此溶液经离心分离可制得固体亚铁。
七、脱销工艺流程说明
1、何为脱硝?所谓脱硝,指的是除去烟气中的NOX,NOX主要是NO和NO2组成,而NO含量占90%以上。要除去烟气中的NO和NO2,就必须研究NO和NO2的性质。
NO是一种惰性氧化物,它虽然溶于水,但不能生成氮的含氧酸。在0℃时,一体积水可溶解0.07体积的NO。NO最特殊的化学性质是加合作用,在常温下能与空气中的氧化合,生成红棕色的NO2。NO是不稳定的,和O2相遇,能使O2分裂成氧原子,并和其中的一个氧原子结合成NO2。
NO2是红棕色有特殊臭味的气体,在-10℃左右聚合成N2O4,在120℃时N2O4全部分解成NO2,温度再高NO2开始分解成NO和O2。NO2是一种强氧化剂,它能把SO2氧化成SO3。NO2溶于水生成硝酸和亚硝酸。NO2的毒性是NO的5倍。
NO和NO2是怎样产生的呢?一般情况下N2和O2不发生化合反应。氮氧化合物是在空气中放电时或在高温燃烧过程中产生的,首先生成NO,然后由NO氧化成NO2。在高温燃烧过程中空气中的氮和燃料中的氮化物等不可能燃烧的物质与氧起化学反应,首先形成NO,随后它的一部分在烟道内与氧化合形成NO2,大部分的NO从烟囱中排入大气,并与大气中的氧结合成NO2。而未被氧化成NO2的NO就在大气中与NO2共存下来。
在燃烧过程中燃烧气体温度越高,过剩空气越多,形成NO量就越多。即在燃烧效率越高的情况下,NO越容易生成。这种燃烧方式生成的NOX中NO占90%以上,NO2较少。
按照常用的燃烧方式。煤的燃烧物中NOX的含量为500-1500ppm。
2、湿法脱硝
脱硝方法分为干法和湿法两种。干法脱硝效率在80%左右,且成本较高。这里采用湿法脱硝。
NO2溶于水生成硝酸和NO:
3NO2+H2O=2HNO3+NO
当氧气足够时:
4NO2+O2+2H2O=4HNO3
NO虽然溶于水,但不能生成氮的含氧酸。在0℃时,一体积水可溶解0.07体积的NO。NO难溶于水成为脱硝的难点。但在“脱硫脱硝除尘一体化技术”中有足够的水使NO溶于水中,有关研究表明当水溶液中硝酸含量>12%时,NO的溶解度比在纯水中大100倍,即一体积水能溶解7体积的NO。设烟气开始溶于水中时水是纯净,首先是NO2溶于水中生成HNO3,如果NO2在水中不被还原,按照“脱硫脱硝除尘一体化技术”中烟水的比例计算,2小时44分钟后,水溶液中硝酸的含量将为12%左右。因此可以说NO溶于水中是不成问题的。
NO和NO2既然都已溶于水中。采用还原法将它们还原成N2气。还原法使用的还原剂为(NH4)2SO3和NH4HSO3,它们正是氨法脱硫工艺中的产物。还原剂就已在溶液中,脱硝就已经在均匀溶解器中悄悄地进行着。因为NOX在烟气中的数量都很小,还原剂(NH4)2SO3和NH4HSO3的数量是足够的。如果NOX的数量不能全部被还原,剩余的部分将变成NH4NO3被留在溶液中和(NH4)2SO4一起被从溶液中分离出来做为化肥。它们化学反应方程式为:
2NO+O2=2NO2+27千卡
NO+NO2+H2O=4HNO2
NO2+2H2O=HNO2+HNO3
4NO2+O2+2H2O=4HNO3
NH3+HNO3=NH4NO3
NH3+HNO2=N2+2H2O
NH4OH+HNO3=NH4NO3+H2O
NH4OH+HNO2=N2+3H2O
|
NO+NO2+3(NH4)2SO3=N2+3(NH4)2SO4 NO+NO2+3NH4HSO3=N2+3NH4HSO4 4NO2+H2O+3(NH4)2SO3=N2+3(NH4)2SO4+2HNO3 |
|
4NO2+H2O+3NH4HSO3=N2+3NH4HSO4+2HNO3 |
NH4OH+NH4HSO4=(NH4)2SO4•H2O
3、脱硫脱硝除尘效果
1)脱硫率:98%
2)脱硝率:90%
3)除尘效率:100%
八、技术工艺特点
(1)造价和运行费用极低,运行管理工作量极少。
(2)工艺简单,可实现全程自动化控制。
(3)测控参数少(PH值、温度、液位),测控技术成熟。
(4)各流程均有成熟技术可借鉴。
(5)适合各种规模的电站及工业锅炉。
(6)对各种含硫煤(油)具有较好的适应性。
(7)对燃烧装置无不良影响,生产工艺、原料来源及产物应用对周边企业无依赖性。
(8)有利于烟气余热的吸收和利用。
(9)不造成(水体、噪声、粉尘等)二次污染。
(10)脱硫脱硝除尘在同一个装置内完成。一次性投资,脱硫率98%,脱硝率90%以上,除尘率100%,均可进行达标排放。
(11)运行费用低。比传统脱硫方法降低运行费用50%-80%左右。
九、烟气脱硫降低费用
目前的烟气脱硫技术存在最大的问题是技术复杂,造价高,运行费用大。一台300MW(30万千瓦)发电机组烟气脱硫,一般采用比较成熟的石灰石--石膏湿法烟气脱硫,脱硫效率95%左右,每年减少二氧化硫排放量约1万吨,每脱除1万吨二氧化硫的能力建设投资约1~1.5亿元,电厂烟气脱硫设施的运行耗电量较大,一年的脱硫剂、用电和人工等运行费在1600万元左右,摊到每度电的脱硫费用约0.03元,而上网电价的脱硫补贴只有0.015元。现时几十吨的锅炉多数用双碱法,近年烧碱(用作烟气脱硫剂)的销售价成倍提高,脱硫运行费用随之大幅度升高。在煤价升幅50%多和竞价上网的双重压力下,加上脱硫补贴缺口大,高成本的脱硫设施能否坚持正常运行面临严峻的考验。
我国脱硫产业常常面临脱硫运行成本高,国家补贴的脱硫电价,无法使脱硫装置保本运行,采用本技术后,能使目前脱硫系统因运行成本高而停用的SO2净化设备进行运转,真正实现脱硝运行费用“零”投资,无成本,大幅度降低运行费用,大量节约水资源,节约电厂传统脱硫技术因磨损大、结垢严重、系统复杂、配套设备多、维护工作量大,和脱硫系统因(石灰乳法)脱硫堵塞、结垢、腐蚀、磨损、运行费用高、耗电量大给厂内造成的巨大损失,真正实现节能减排,提高效益,可取消浆液循环泵,取消氧化风机,取消制浆系统,取消石灰石球磨机等,大大节约系统的用电量,本脱硫方法与传统的(石灰乳)脱硫方法相比,脱硫效率98%以上,脱硝效率90%以上,可降低运行费用50%-80%,是脱硫领域的一次创新和一项重大突破,在国内外尚属首创。无论对低硫煤、中硫煤、高硫煤,均能达到与传统(石灰乳)法脱硫相当的效果,实现脱硫系统运行费用零投资,无成本脱硫,脱硫塔排出的吸收液,重复利用,循环脱硫,即节约了大量的水资源,又减少了脱硫系统设备系统管道的堵塞和结垢,省去了传统湿法脱硫工艺中庞大的制浆系统,省去了废液和废水处理设备,整套系统大为简化,设备投资大为降低。
十、烟气脱硫技术对比
与传统的石灰乳脱硫方法脱硫相比,即解决了用水量大,浪费水资源,系统容易结垢、堵塞等问题,又可解决脱去烟气中SO2的问题,一举两得,脱硫效率97%以上,脱硝效率90%以上,除尘率100%,不需大的投资建设脱硝设备,无成本,大幅度降低运行费用,提高经济效益,真正实现节能减排,循环经济,变废为宝,实现国家可持续发展。
十一、社会经济意义
湿法脱硫技术是最具商业优势的脱硫技术,“脱硫脱硝除尘一体化技术”使(湿法)烟气脱硫设备及装置的小型化、普及化成为可能,使治理SO2污染在一些经济条件较差的国家和地区的普及应用成为可能。它的经济、高效、节能、环保、集控的特点和优点有利于为众多企业所接受,为经济的可持续发展和环境科技的进步做出应有的贡献。










